Biografia di Amedeo Avogadro | Scienziati famosi.

Nota: Questa traduzione è fornita per scopi educativi e potrebbe contenere errori o essere impreciso.
Vissuto 1776 – 1856.
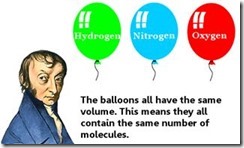
Amedeo Avogadro è meglio conosciuto per la sua ipotesi che volumi uguali di gas differenti contengono lo stesso numero di molecole, purché siano alla stessa temperatura e pressione.
Sua ipotesi è stata rifiutata da altri scienziati. Ha guadagnato solo dopo la sua morte. Ora è chiamato legge di Avogadro.
Fu anche il primo scienziato a rendersi conto che gli elementi potrebbero esistere sotto forma di molecole piuttosto che come singoli atomi.
Vita di Avogadro
Amedeo Avogadro è Nato a Torino, il 9 agosto 1776.Suoi rapporti famigliari era aristocratica. Suo padre, Filippo, era un magistrato e senatore che aveva il titolo di Conte. Sua madre era una nobildonna, Anna Vercellone di Biella.
Amedeo Avogadro ereditò il titolo di Conte da suo padre. Infatti, il nome completo di Amedeo Avogadro era Conte Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e di Cerreto – un bel boccone!
Avogadro era molto intelligente. Nel 1796, quando aveva solo 20, ottenne un dottorato in diritto canonico e iniziò a praticare come avvocato ecclesiastico.
Anche se aveva seguito la tradizione di famiglia studiando legge, ha gradualmente perso interesse in materia giuridica. Ha trovato la scienza era molto più intellettualmente stimolante.
Matematica e fisica in particolare ha attirato la sua mente logica. Ha speso una quantità crescente di tempo a studiare queste materie. Fu aiutato in questo dal fisico matematico prominente professore Vassalli Eandi.
Nel 1803, in collaborazione con suo fratello Felice, Avogadro pubblicato il suo primo lavoro scientifico, che ha esaminato il comportamento elettrico di soluzioni saline. Questo era stato-of-the-art Scienza: solo tre anni prima, compagni italiani scienziato di Avogadro Alessandro Volta aveva dimostrato la batteria elettrica per la prima volta.
Nel 1806, 30 anni, Avogadro abbandonato la sua attività di avvocato di successo e ha cominciato ad insegnare matematica e fisica presso un liceo a Torino. Nel 1809 divenne un senior teacher presso il Collegio di Vercelli.
Nel 1820 Avogadro è diventato il professore di fisica matematica presso l'Università di Torino. Purtroppo, questo post fu di breve durata a causa di disordini politici. Avogadro ha perso il lavoro nel 1823.
Avogadro è stato riconfermato nel 1833 e mantenne questo posto fino a quando, all'età di 74, si ritirò nel 1850.
Anche se lui era un aristocratico, Avogadro era un uomo terra-terra, privato, che era in silenzio religioso. Gli è stato dedicato al duro lavoro e il suo stile di vita era semplice. Sua moglie si chiamava Felicita Mazzé. Si sono sposati nel 1818 quando Avogadro era invecchiato 42. Ebbero sei figli.
Contributi di Avogadro alla scienza
Nel 1800s iniziale, idee degli scienziati sulle particelle che oggi chiamiamo atomi e molecole erano molto limitate e spesso errate. Avogadro era profondamente interessato a scoprire come le particelle fondamentali della materia si sono comportati e si sono riuniti per formare composti chimici.Ha studiato il lavoro di altri due scienziati:
1. John Dalton
Nel 1808 John Dalton pubblicò la sua teoria atomica proponendo che tutta la materia è fatta di atomi. Dichiarò inoltre che tutti gli atomi di un elemento sono identici, e gli atomi di elementi diversi hanno masse diverse. In tal modo, Dalton ha trasportato chimica ad un nuovo livello. Ma ha anche fatto errori sugli elementi del modo si combinano per formare composti. Ad esempio, ha pensato di acqua era costituito da un atomo di idrogeno e un atomo di ossigeno e ha scritto come HO; oggi sappiamo che l'acqua contiene due atomi di idrogeno per ogni ossigeno e scriviamo acqua come H20. In realtà, Avogadro calcolato questo fuori, come vedremo.2. Joseph Gay-Lussac
Nel 1809 Joseph Gay-Lussac pubblicato sua legge della combinazione di volumi di gas. Aveva notato che quando due litri di gas idrogeno reagiscono con un litro di gas ossigeno, formano due litri di acqua gassosa. Tutti i gas che ha reagito sembravano reagire in rapporti di volume semplice.Ipotesi di Avogadro
Nel 1811 Avogadro ha pubblicato un documento nel Journal de Physique, la francese Journal of Physics. Ha detto che la migliore spiegazione per le osservazioni di Gay-Lussac delle reazioni di gas era che volumi uguali di tutti i gas alla stessa temperatura e pressione contengono lo stesso numero di molecole. Questo è ora chiamato legge di Avogadro. Lo pubblicò quando stava lavorando come insegnante di fisica al liceo di Vercelli.Nella visualizzazione (corretto) di Avogadro, il motivo che due litri di gas idrogeno reagiscono con un litro di gas di ossigeno per formare solo due litri di acqua gassosa è che il volume diminuisce perché il numero di particelle presenti diminuisce. Deve pertanto la reazione chimica:
2H2 (gas) + O2 (gas) → 2 H20 (gas)
In questa reazione tre particelle (due molecole di idrogeno e ossigeno di una molecola) vengono insieme per formare due particelle d'acqua... o 200 particelle reagiscono con 100 particelle per formare 200 particelle... o 2 milioni di particelle reagiscono con 1 milione di particelle per formare particelle di 2 milioni... ecc. L'effetto osservabile è che dopo la reazione, quando tutti di gas idrogeno e ossigeno sono diventati H20 gas, il volume di gas cade a due terzi del volume iniziale.
Come conseguenza di queste osservazioni Avogadro è diventato il primo scienziato a rendersi conto che gli elementi potrebbero esistere come molecole piuttosto che come singoli atomi. Ad esempio, ha riconosciuto che l'ossigeno intorno a noi esiste come una molecola in cui sono legati due atomi di ossigeno.
Altri scienziati nel campo, ad esempio Dalton, credevano che solo composti potrebbero formare molecole, mentre tutti gli elementi hanno esistito come singoli atomi.

Avogadro realizzato che elementi potrebbero esistere sotto forma di molecole con singoli atomi uniti insieme.
Nel 1815 Avogadro ha pubblicato un ulteriore documento in Journal de Physique discutendo le masse degli atomi, la loro composti e la loro densità del gas.
Nel 1821, ora scrivendo come il professore di fisica matematica presso l'Università di Torino, ha pubblicato un ulteriore documento guardando le masse degli atomi e le proporzioni in cui si combinano.
Tra il 1837 e il 1841 Avogadro ha pubblicato quattro volumi pesanti alla ricerca in dettaglio la fisica della materia.
I risultati di Avogadro sono stati quasi completamente ignorati fino a Stanislao Cannizarro loro presentato al Congresso di Karlsruhe nel 1860, quattro anni dopo la morte di Avogadro. Questa conferenza era stata chiamata per risolvere la confusione scientifica che esisteva circa atomi, molecole e le loro messe.
Anche dopo Cannizarro presentato il suo lavoro che non tutti gli scienziati concordati con esso. Un altro decennio passato – con continuo sostegno forte da Cannizarro – prima ipotesi di Avogardo divennero più largamente accettata e divennero legge di Avogadro.
Avogadro è oggi considerato come uno dei fondatori della chimica atomico-molecolare.
Perché è stata rifiutata la ipotesi di Avogadro per decenni?
Ci sono una serie di motivi perché lavoro di Avogadro non è stato accettato rapidamente:• Pubblicò la sua opera in Journal de Physique, che non era un giornale molto ben leggere.
• Le teorie di meglio noti scienziati del tempo, come John Dalton e Jöns Jacob Berzelius, in disaccordo con il lavoro di Avogadro.
• Italia – il paese di Leonardo da Vinci e Galileo – non fu considerato non più come un paese dove è stato fatto grande scienza. Comprendendo questo, pochi anni prima, compatriota di Avogadro Alessandro Volta aveva viaggiato fuori dall'Italia per rendere se stesso e il suo lavoro noto agli scienziati di altri paesi. Avogadro, ha soggiornato in Italia e non fanno contatto personale con scienziati stranieri per aiutare a colmare il divario, come aveva fatto la Volta.
Anche se ci piace pensare di scienza come un nobile sforzo, dove la verità diventerà presto evidente, che questo non è sempre il caso. Gli scienziati sono solo persone; possono essere testardi, proprio come tutti noi possiamo essere a volte. Se si dispone di una nuova teoria scientifica controversa, e non si è ben noto, sembra che contatto personale a volte può raggiungere tanto quanto un paper scientifico – o anche di più.
La costante di Avogadro
Costante di Avogadro è uno dei numeri più importanti nella chimica. Il suo valore è 6.02214129 x 1023. Avogadro non ha calcolato questo numero, ma la sua esistenza consegue logicamente dalla sua ipotesi e lavoro.Costante di Avogadro è il numero di particelle (atomi o molecole) in una mole di qualsiasi sostanza. Ad esempio, 12 grammi di carbonio contengono 6.02214129 x 10 atomi di carbonio di23 .
Costante di Avogadro è un numero enorme. Se si potrebbe risparmiare 1 milione di dollari un secondo, ci vorrebbero più di quanto l'universo è creduto per essere esistito per salvare 6.02214129 x 1023 dollari; che tutto va a dimostrare che ci vuole un sacco di atomi per fare una piccola quantità di materia!
"Gli studi delle scienze naturali hanno particolarmente coinvolto quella parte della fisica che studia il mondo atomico: le proprietà delle molecole, le forze coinvolte nel loro movimento, la capacità termica delle sostanze differenti, dilatazione dei gas dal calore e la densità e pressione dei gas."
Amedeo Avogadro, 1776 – 1856